Wikisage is op 1 na de grootste internet-encyclopedie in het Nederlands. Iedereen kan de hier verzamelde kennis gratis gebruiken, zonder storende advertenties. De Koninklijke Bibliotheek van Nederland heeft Wikisage in 2018 aangemerkt als digitaal erfgoed.
- Wilt u meehelpen om Wikisage te laten groeien? Maak dan een account aan. U bent van harte welkom. Zie: Portaal:Gebruikers.
- Bent u blij met Wikisage, of wilt u juist meer? Dan stellen we een bescheiden donatie om de kosten te bestrijden zeer op prijs. Zie: Portaal:Donaties.
Tin (element)
 Zie ook : tin (doorverwijzing), voor andere betekenissen en toebehoren van "tin".
Zie ook : tin (doorverwijzing), voor andere betekenissen en toebehoren van "tin".
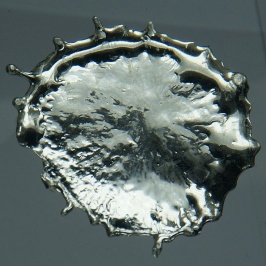
Tin oftewel Stannum is een scheikundig element met symbool Sn en atoomnummer 50. Het is een zilvergrijs hoofdgroepmetaal.
Ontdekking
Tin, één van de vroegst ontdekte metalen, werd veelal in brons gebruikt. In 3500 v.Chr. was al bekend dat tin (evenals arseen en nikkel) een verhardend effect had op koper. Daarom werd het gebruikt in gereedschappen en wapens.
Al voor de tijd van de Romeinen ontstond er een bloeiende handel tussen de tinmijnen in Cornwall en het Middellandse Zeegebied. De Egyptische farao Pepi heeft rond 2300 v.Chr. een standbeeld laten maken waarin tin zat uit de tinmijnen van Cornwall.
Vanaf ongeveer het jaar 600 werd tin ook in zuivere vorm toegepast.
Het woord tin komt van het Germaans *tina- en staat ablautend naast teen dat 'twijg' en in het Duits (Zain) ook 'metalen staaf' betekent. Het symbool Sn komt van het neolatijn stannum dat van het postklassieke Latijn stagnum 'legering van zilver en lood' komt.
Toepassingen
Tin hecht zich gemakkelijk aan ijzer en wordt daardoor vaak gebruikt als roestwerende coating (blik). Andere toepassingen zijn:
- Legering met lood voor Orgelpijpen.
- In bronslegeringen voor kerkklokken.
- Als zachte soldeertin voor de productie van elektronische schakelingen en loodgieterswerk.
- Het zout tinchloride wordt gebruikt als bijtmiddel.
- Om glas een glad oppervlak te geven wordt het vaak in vloeibare vorm op tinnen platen gegoten (het proces van Pilkington).
- Gesmolten tin wordt door een tingieter in vormen gegoten voor de vervaardiging van gebruiksvoorwerpen (oud bestek) of siervoorwerpen (tinnen soldaatjes).
- In vroeger eeuwen werd tin vaak gebruikt om borden, bekers, kannen e.d. te maken. (Sinds de 18e eeuw is het tinnen tafelgerei wat in onbruik geraakt en vervangen door porselein, aardewerk en glas).
- In de legering Woodsmetaal voor diverse toepassingen.
De naam tin wordt in het Engels soms foutief gebruikt voor dunbladige metalen. Het tinnen blikje is daar het beste voorbeeld van omdat blikjes worden vervaardigd van aluminium of van staal dat met een dun laagje tin tegen roestvorming wordt beschermd.
Opmerkelijke eigenschappen
Tin is een buigzaam, kneedbaar en zeer kristallijn zilverachtig-wit metaal dat bij buiging een karakteristiek geluid geeft dat wordt veroorzaakt door de brekende kristallen. Het metaal is bestand tegen zee- en kraanwater, maar is oplosbaar in de meeste zuren.
Bij standaarddruk komen er twee allotropen van tin voor. Bij lage temperatuur komt het voor als grijs - alfa - tin met een kubische kristalstructuur vergelijkbaar met die van silicium en germanium. Bij temperaturen boven de 13,2 °C verandert het naar wit - beta - tin. In deze vorm heeft het een tetragonale structuur. Bij afkoeling keert het weer terug naar de kubische vorm. Vroeger werd dit proces wel tinpest genoemd; het kan worden voorkomen door toevoeging van antimoon of bismut.
Verschijning
Op vrijwel alle continenten op aarde komt tin voor. Het erts wordt bij hoge temperatuur in ovens gereduceerd met koolstof. Het enige commercieel aantrekkelijke tinbevattende mineraal is cassiteriet, dat vooral in Zuidoost-Azië in ruime mate gevonden wordt. Andere mineralen die in lage concentraties tin bevatten zijn: stanniet, cylindriet, frankeiet, canfieldiet en tealliet.
Isotopen
| Meest stabiele isotopen | |||||
|---|---|---|---|---|---|
| Iso | RA (%) | Halveringstijd | VV | VE (MeV) | VP |
| 112Sn | 0,97 | stabiel met 62 neutronen | |||
| 114Sn | 0,65 | stabiel met 64 neutronen | |||
| 115Sn | 0,34 | stabiel met 65 neutronen | |||
| 116Sn | 14,54 | stabiel met 66 neutronen | |||
| 117Sn | 7,68 | stabiel met 67 neutronen | |||
| 118Sn | 24,22 | stabiel met 68 neutronen | |||
| 119Sn | 8,58 | stabiel met 69 neutronen | |||
| 120Sn | 32,59 | stabiel met 70 neutronen | |||
| 121Sn | syn | 27,06 u | β | 3,674 | 121Sb |
| 122Sn | 4,63 | stabiel met 72 neutronen | |||
| 124Sn | 5,79 | stabiel met 74 neutronen | |||
| 126Sn | syn | 1×105 j | β | 8312 | 126Sb |
Van alle elementen komen er van tin de meeste stabiele isotopen voor (10). Daarnaast zijn er ongeveer 18 radioactieve isotopen bekend.
Toxicologie en veiligheid
Via blikvoeding krijgen mensen lage concentraties tin binnen. Tot op heden zijn daarvan geen schadelijke gevolgen bekend en dus kan worden gesteld dat tin ongevaarlijk is. Rond 1965 steeg de tinprijs exponentieel (tot 45 euro per kilogram, nu: 5 euro per kilogram), waardoor vele tingieters om de kostprijs te drukken hun legering met lood aanlengden. Als uit zo'n tinnen beker gedronken werd liep men uiteraard het risico van loodvergiftiging.
Externe links
- PeriodiekSysteem.com over: Tin
- Lenntech over: Tin
- (en) EnvironmentalChemistry.com over: Tin
- (en) WebElements.com over: Tin
| Chemische elementen en isotopen |
|---|
|
Periodiek systeem: Standaard · Alternatief · Elektronenconfiguratie |